Piano strategico di ricerca 2021-24
L’associazione AILE, insieme alla comunità di sostenitori e a tutte le parti interessate, promuove attraverso la collaborazione con la comunità scientifica un programma di finanziamenti che possa accelerare le scoperte mediche per la cura dei malati di HLH familiare e secondaria. A tale proposito, AILE ha sviluppato un piano strategico di ricerca per i prossimi 3 anni (2021-2024) per promuovere in modo significativo la ricerca traslazionale con i seguenti scopi:
- La ricerca clinica
- La conoscenza capillare sul territorio della HLH
- La ricerca terapeutica
- L’acquisizione di conoscenza dei meccanismi genetici e patologici
LA RICERCA CLINICA
La necessità invocata da molti ricercatori di poter avere degli studi clinici prospettici che permettano di capire le cause della HLH primaria e secondaria e di poterne stimare l’incidenza, spinge AILE a cercare collaborazioni e supportare finanziariamente gruppi nazionali e internazionali che possano realizzare questi studi scientifici da cui dipendono il miglioramento della salute e lo sviluppo a lungo termine di terapie innovative. Nello scorso triennio l’associazione ha istaurato contatti con organizzazioni internazionali e con l’industria farmaceutica che ha permesso di finanziare di un progetto di ricerca clinica sulle complicazioni da rigetto del trapianto di cellule staminali.
Oltre a monitorare e sostenere questo primo successo, AILE si impegna nel prossimo triennio a patrocinare studi clinici per identificare nuovi trattamenti e/o combinazioni terapeutiche che diano risultati ottimali soprattutto nei malati di HLH con meccanismi patologici differenti o multipli.
Il disporre di un registro mondiale per la HLH permetterebbe di capire meglio lo spettro già ampio di caratteristiche cliniche/patologiche con cui la sindrome si manifesta e determinare le aree di ricerca da sviluppare e necessarie per migliorare le terapie e quindi la qualità di vita dei pazienti. AILE sosterrà la creazione di un registro italiano e collaborerà attivamente a quello internazionale, già esistente.
LA CONOSCENZA DELL’HLH
La conoscenza dell’HLH a tutti i medici anche al di fuori del circuito specialistico, è fondamentale per permettere ad ogni singolo paziente di essere preso in carico dagli ospedali di riferimento e di ricevere le adeguate cure. Infatti è fondamentale il riconoscimento della sindrome HLH per migliorare l’accesso a test specifici e quindi ridurre al minimo i ritardi nella diagnosi/trattamento e quindi l’alta mortalità di questa patologia.
Nel piano strategico precedente l’associazione si è impegnata a diffondere la conoscenza dell’HLH attraverso la pubblicazione sul suo sito web di blog scientifici inerti alla malattia e il finanziamento ai ricercatori con il “Premio al Miglior Articolo Scientifico”. Queste azioni verranno mantenute anche nel prossimo triennio e verranno istituite campagne di consapevolezza sulla malattia per raggiungere i medici ospedalieri e quelli di base e far in modo che HLH possa essere riconosciuta e identificata già agli esordi.
LA RICERCA TERAPEUTICA
Gli sforzi della comunità scientifica hanno prodotto nuove terapie che vengono attualmente saggiate per la loro efficacia. AILE vuole promuovere e sostenere la scoperta di nuovi medicinali che permettano di ridurre la mortalità e favorire la guarigione dei malati. Per questo l’associazione patrocina progetti che abbiamo lo scopo di identificare i meccanismi immunitari fondamentali, in particolare quelli che portano alla HLH Neurologica, e che permettano lo sviluppo di terapie per il controllo dell’iper-attivazione del sistema immunitario.
Dato che la terapia genica ha il potenziale di revertire il fenotipo genetico alla base della HLH familiare, AILE si fa promotore di ricerche per la caratterizzazione di difetti genetici nei pazienti, la creazione di modelli animali e lo sviluppo di nuovi strumenti diagnostici e di trattamento ed infine, si propone di stimolare programmi di ricerca sulla terapia genica.
L’ACQUISIZIONE DI CONOSCENZA DEI MECCANISMI GENETICI E PATOLOGICI
Per migliorare le terapie per i pazienti HLH abbiamo bisogno di capire i meccanismi patogenetici di questa sindrome. Dati scientifici dimostrano sempre più che il termine HLH indica una manifestazione patologica ampia che comprende sia pazienti pediatrici, che soffrono di un numero sempre più ampio di malattie genetiche, e non, in cui l’HLH è una complicanza rara di un disturbo primario causato da altri difetti genetici, compresi deficienze immunitarie primarie ed errori congeniti del metabolismo. Inoltre l’HLH si può verificare in pazienti con sindromi reumatologiche e/o infiammatorie e in pazienti durante infezioni o neoplasie senza una nota (o non ancora identificata) predisposizione genetica.
Tale eterogeneità ha bisogno di essere studiata nei dettagli e sicuramente il sequenziamento genomico è stato e sarà di grande aiuto nella conoscenza dell’HLH. AILE favorisce perciò studi scientifici di tipo meccanicistico per meglio comprendere la complessità della sindrome e definire le caratteristiche patologiche in modo da stabilire una miglior correlazione tra fenotipo /genotipo.
Premio per il Miglior Articolo Scientifico 2024
AILE bandisce due premi per il Migliore Articolo Scientifico, su tematiche concernenti la Linfoistiocitosi Emofagocitica, in memoria di Mario Ricciardi. A questo scopo, è indetta una procedura selettiva per l’attribuzione dei premi per due articoli scientifici pubblicati nel biennio 2022-2023.
Bando per la ricerca 2024 - Concluso
L’Associazione annuncia la disponibilità di fondi per sostenere ricerche scientifiche innovative.
Questa progettualità mira a sostenere progetti finalizzati a nuovi trattamenti per alleviare i sintomi della HLH.
Premio Mario Ricciardi 2022

L’Associazione AILE bandisce 2 premi per il Migliore Articolo Scientifico, su tematiche concernenti la Linfoistiocitosi Emofagocitica, in memoria di Mario Ricciardi.
A questo scopo, è indetta una procedura selettiva per l’attribuzione dei premi per due articoli scientifici pubblicati nel biennio 2020-2021.
A.I.L.E. Association announces 2 awards for the Best Scientific Article, on issues concerning Hemophagocytic Lymphohistiocytosis (HLH), in memory of Mario Ricciardi. A selective procedure for two scientific articles published during the 2020-2021 is announced.
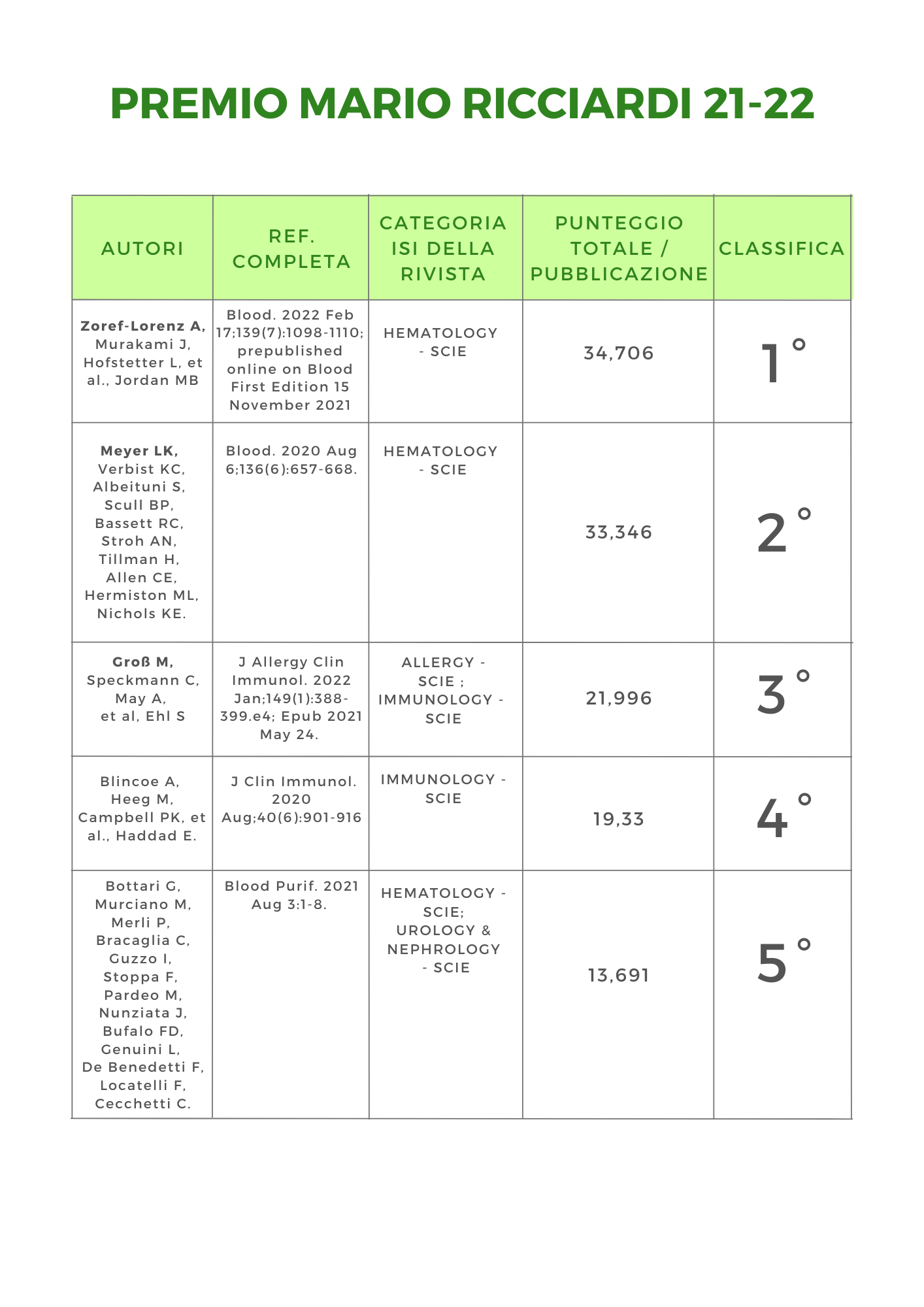
Visualizza la classifica punteggi dei partecipanti al premio Mario Ricciardi 2022 cliccando sul pulsante in basso.
VINCITORI
La Seconda Edizione del Premio Internazionale al miglior articolo scientifico (2019-2021) si è recentemente conclusa con la pubblicazione della classifica, stilata secondo parametri internazionali, che permettono di valutare la qualità scientifica (impact factor) degli articoli sottomessi. I vincitori dei due premi sono due giovani ricercatrici che lavorano presso la Clinica Universitaria del Cincinnati Children’s Hospital, (USA) e la Pediatria dell’Ospedale St Jude di Memphis (USA).
Abbiamo chiesto alle vincitrici un contributo scritto che evidenzi in che modo i loro risultati pubblicati siano importanti per migliorare la conoscenza dell’HLH. Ecco il loro contributo:

Dr.ssa Lorenz Adi 1° classificata.
1° Classificata Dr. Lorenz Adi
Zoref-Lorenz, Adi et al. “An improved index for diagnosis and mortality prediction in malignancy-associated hemophagocytic lymphohistiocytosis.” Blood vol. 139,7 (2022): 1098-1110
| La clinica pediatrica di Cincinnati e di Memphis sede delle ricerche pubblicate dalle ricercatrici vincitrici del premio. |
Hemophagocytic lymphohistiocytosis (HLH) is a hyperinflammatory syndrome for which hematologic malignancy (HM) is a common and deadly trigger. The paper- “An improved index for diagnosis and mortality prediction in malignancy-associated hemophagocytic lymphohistiocytosis” describes our study of 225 adult patients with HM with and without HLH by the HLH-2004 criteria. We report that combined elevation of soluble CD25 and ferritin at optimized cutoff values defines an optimized HLH inflammatory (OHI) index that accurately identifies patients fulfilling HLH criteria; however, more importantly, it also predicts high mortality risk whether or not patients fulfill HLH criteria. The OHI index is important as it will allow early identification of the syndrome and deeper investigation into its pathophysiology.
La Linfoistiocitosi Emofagocitica (HLH) è una sindrome iperinfiammatoria, in cui il tumore maligno ematologico (HM) rappresenta un fattore scatenante comune e mortale. L’articolo “Un indice migliorato per la diagnosi e la previsione della mortalità nella linfoistiocitosi emofagocitica associata a malignità” descrive il nostro studio su 225 pazienti adulti con HM con e senza HLH definita secondo i criteri HLH-2004. Segnaliamo che l’aumento combinato nel sangue del CD25 solubile e ferritina a valori di cutoff ottimizzati definisce un indice infiammatorio HLH ottimizzato (OHI) che identifica accuratamente i pazienti che soddisfano i criteri HLH; tuttavia, cosa ancora più importante, predice anche un alto rischio di mortalità indipendentemente dal fatto che i pazienti soddisfino o meno i criteri HLH. L’indice OHI è importante in quanto consentirà l’identificazione precoce della sindrome e un’indagine più approfondita nella sua fisiopatologia.

Dr.ssa Meyer Lauren 2° classificata, St. Jude Hospital, Memphis, USA
2° Classificata Dr. Meyer Lauren
Meyer, Lauren K et al. “JAK/STAT pathway inhibition sensitizes CD8 T cells to dexamethasone-induced apoptosis in hyperinflammation.” Blood vol. 136,6 (2020): 657-668.
|
Per ulteriori informazioni su questa pubblicazione, consultare l’articolo di ottobre 2021 sul nostro sito cliccando qui o sfogliando articoli in evidenza in basso. |
HLH therapy relies heavily on the anti-inflammatory activity of dexamethasone, but many patients are refractory to this therapy. Hypercytokinemia is a hallmark of HLH, and many cytokines activate the pro-survival JAK/STAT signaling pathway in immune cells. We hypothesized that cytokine exposure might antagonize dexamethasone-induced apoptosis. Using in vitro and in vivo models, we found that cytokines alter the apoptotic potential of immune cells, rendering them resistant to dexamethasone. However, simultaneous exposure to the JAK1/2 inhibitor ruxolitinib greatly potentiated dexamethasone-induced apoptosis with a concomitant improvement in disease manifestations in our in vivo model.
La terapia dell’HLH si basa principalmente sull’attività antinfiammatoria del desametasone, ma molti pazienti non rispondono a questa terapia. L’elevato livello di citochine nel sangue è un segno distintivo dell’HLH e molte citochine attivano la via di segnale JAK/STAT che favorisce la sopravvivenza delle cellule immunitarie. Abbiamo ipotizzato che l’esposizione delle cellule immunitarie ad elevati livelli di citochine potrebbe antagonizzare l’apoptosi indotta dal desametasone. Utilizzando modelli in vitro e in vivo, abbiamo scoperto che le citochine alterano il potenziale apoptotico delle cellule immunitarie, rendendole resistenti al desametasone. Tuttavia, l’esposizione simultanea all’inibitore JAK1/2 ruxolitinib ha notevolmente potenziato l’apoptosi indotta da desametasone con un concomitante miglioramento delle manifestazioni della malattia nel nostro modello in vivo.
ARTICOLI IN EVIDENZA SUL PREMIO MARIO RICCIARDI
Partecipanti al Premio “Mario Ricciardi” (Seconda edizione)
La Seconda Edizione del Premio Internazionale al miglior articolo scientifico pubblicato dal 2019 al 2021 oltre alle ...
L’uso di Anticorpi sintetici per il controllo dell’iperinfiammazione mediata da interferone gamma nell’HLH e nel COVID19
Le analogie dell'iperinfiammazione da HLH e COVID19 Negli ultimi due anni, molti termini medici riferiti alle malattie...
Bandi di ricerca

BANDO PER LA RICERCA 2021
L’Associazione Italiana Linfoisticitosi Emofagocitica (AILE), organizzazione no profit per la promozione ed il sostegno della ricerca scientifica nel trattamento della sindrome della Linfoisticitosi Emofagocitica (HLH), annuncia, insieme a Sobi s.r.l., affiliata italiana dell’azienda farmaceutica svedese, impegnata nella cura di malattie immunologiche rare, la disponibilità di fondi per sostenere ricerche scientifiche innovative. Questa progettualità mira a sostenere progetti finalizzati a nuovi trattamenti per alleviare i sintomi della HLH.
L’ area tematica, identificata tra le priorità di finanziamento, è quella del:
RIGETTO DEL TRAPIANTO ALLOGENICO di cellule staminali
Il progetto di ricerca vincitore è “Deep profiling of graft failure after allogeneic HSCT” del Dott. Pietro Merli del Dipartimento di Oncoematologia, Terapia Cellulare, Terapie Geniche e Trapianto Emopoietico dell’IRCCS Ospedale Pediatrico Bambino Gesù di Roma.
È fondamentale approfondire i diversi meccanismi che possono concorrere al rigetto del trapianto di cellule staminali ematopoietiche – spiega Merli – perché ad oggi, a differenza del trapianto di organo solido, non esistono terapie efficaci per trattare un rigetto incipiente e la linfoistiocitosi emofagocitica primaria presenta un rischio aumentato di rigetto. Così, questo progetto di ricerca vuole sfruttare le tecnologie più avanzate per caratterizzare il profilo di nuovi marcatori nei liquidi biologici, per esempio nel sangue: l’obiettivo è di sviluppare nuove strategie sia diagnostiche, al fine di anticipare la diagnosi, che purtroppo oggi è spesso tardiva e arriva quando ormai il rigetto si è già completato, che terapeutiche”.
Servizio di Adnkronos sul progetto vincitore.

In collaborazione con

Con il patrocinio non oneroso del

Articoli dei partecipanti
Partecipanti al Premio “Mario Ricciardi” (Seconda edizione)
La Seconda Edizione del Premio Internazionale al miglior articolo scientifico pubblicato dal 2019 al 2021 oltre alle due vincitrici americane ha annoverato il contributo fondamentale di ricercatori...
L’uso di Anticorpi sintetici per il controllo dell’iperinfiammazione mediata da interferone gamma nell’HLH e nel COVID19
Le analogie dell'iperinfiammazione da HLH e COVID19 Negli ultimi due anni, molti termini medici riferiti alle malattie respiratorie quali infezioni virali, sindrome respiratoria acuta, immunità,...
Decima classificata
La Dr. ssa Bracaglia lavora presso la Divisione di Reumatologia, Ospedale pediatrico Bambino Gesù, IRCCS, Roma, Italia. L’articolo proposto per la competizione il Miglior Articolo Scientifico...
Nona classificata
La Dr. ssa Boggio è un medico che lavora alla Scuola di Patologia, Università degli Studi di Milano, Fondazione IRCCS Ca ‘Granda-Ospedale Maggiore Policlinico, Milano, e affiliata presso l�...
Ottavo classificato
Il Dr. Saettini è un medico che lavora presso il Dipartimento di Pediatria, Fondazione Monza e Brianza per il bambino e la Mamma, Università della Milano-Bicocca, Monza. Lavora nel gruppo di Dr. ...
Settima classificata
Il Dr.ssa Prencipe è un medico che lavora presso l’Ospedale Pediatrico Bambino Gesù, Dipartimento di Ematologia / Oncologia pediatrica, terapia cellulare e genica, Roma, diretto dal Prof. Franc...
Sesto classificato
Il Dr.Merli lavora presso l’Ospedale Pediatrico Bambino Gesù, Dipartimento di Ematologia / Oncologia pediatrica, terapia cellulare e genica, Roma, diretto dal Prof. Franco Locatelli. Fa parte ...
Quinta classificata (ex aequo)
La Dr.ssa Panchal è dottoranda presso la Sezione di Immunologia Molecolare e Cellulare, Istituto Pediatrico, Great Ormond Street, Londra, Regno Unito, diretto dal Prof. Persis Amrolia. Il gruppo d...
Quinto classificato (ex aequo)
Il Dr. Volkmer lavora presso la Divisione di Immunologia, della Clinica Universitaria Pediatrica di Zurigo, diretta dal Prof.ssa Jana Pachlopnik Schmid. Il gruppo di ricerca si occupa di studiare l...
Quarto classificato
Il Dr. Liston è group leader al Center for Brain & Disease Research, e al Dipartimento di Microbiologia e Immunologia, dell’Università di Leuven, Belgio. L’articolo presentato si intitola...
Terza classificata
La Dr.ssa Albeituni è una giovane ricercatrice che lavora nel gruppo di ricerca diretto dalla Dott.ssa Nichols Kim del St. Jude Children’s Research Hospital di Memphis: ha partecipato alla c...
Premio Mario Ricciardi 2020
Premio Mario RicciardiL’Associazione AILE Onlus bandisce 2 premi per il Migliore Articolo Scientifico, su tematiche concernenti la Linfoistiocitosi Emofagocitica, in memoria di Mario Ricciardi. A...
Aggiornamenti scientifici
HLH dell’adulto: quale ruolo per il contributo genetico nelle forme secondarie?
HLH dell'adulto: il punto della situazione Nel post di gennaio del blog di AILE abbiamo approfondito le manifestazioni cliniche, le strategie diagnostiche e le opzioni terapeutiche relative alle...
HLH associata a tumori: diagnosi, clinica e terapie
HLH associata a tumori: il punto della situazione La Linfoistiocitosi Emofagocitica associata a tumori (Tumor-associated HLH, T-HLH) richiede particolare attenzione a causa della sua prognosi spesso...
Le linee guida HiHASC: un nuovo strumento per la diagnosi dell’HLH
Nel 2018, nel Regno Unito, è nata una collaborazione clinica con un obiettivo preciso: ridurre la mortalità associata alla Linfoistiocitosi Emofagocitica (HLH). In questo contesto si sviluppa HiHASC...
HLH e neoplasie ematologiche: una combinazione ad alta mortalità
HLH e neoplasie ematologiche: una combinazione ad alta mortalità La gestione clinica della Linfoistiocitosi Emofagocitica (HLH) in pazienti con neoplasie ematologiche rappresenta una delle sfide più...
HLH e CARD11: nuovo meccanismo scoperto nelle cellule dendritiche
Un meccanismo di rinforzo del segnale nelle cellule dendritiche scatena l’iperinfiammazione nella HLH La linfoistiocitosi emofagocitica (HLH) è una malattia infiammatoria sistemica rara e...
Emapalumab nella fHLH: un trattamento ponte verso il trapianto
Emapalumab: un trattamento ponte verso il trapianto di cellule staminali ematopoietiche Emapalumab (Emab), noto con il nome commerciale Gamifant, è un anticorpo monoclonale sviluppato dall'azienda...
Pazienti e caregivers a confronto con i medici per migliorare il percorso diagnostico della HLH
Introduzione Il gruppo di ricercatori, coordinati dal Dr. Donohue, ha evidenziato le difficoltà incontrate dai pazienti nel vedere riconosciuta la Linfoistiocitosi Emofagocitica (HLH) come malattia,...
Nuovi dati dal registro Italiano sulla Linfoistiocitosi Emofagocitica familiare
Cos'è la Linfoistiocitosi Emofagocitica La HLH primaria o familiare (fHLH) è una malattia causata da alterazioni di geni coinvolti nel rilascio dei granuli citotossici dalle cellule immunitarie. La...
Nuovo progresso della terapia genica nella cura della HLH familiare
La terapia La terapia genica della HLH familiare (fHLH) è la nuova frontiera della medicina moderna che promette di rivoluzionare i protocolli di cura per una risoluzione rapida e definitiva della...
Identificata una nuova proteina coinvolta nell’attività di degranulazione delle cellule immunitarie e che predispone alla HLH
La scoperta La nuova scoperta parte dalla storia di due fratelli di Amburgo in Germania nati da genitori consanguinei. Il primo muore a soli due anni di età di HLH a causa di una infezione da...
Un nuovo approccio all’analisi di varianti germinali predice le conseguenze funzionali di mutazioni di significato incerto
Come si effettua l'identificazione delle varianti germinali Una delle sfide nella HLH familiare (fHLH) è sicuramente quella di giungere ad una rapida ed accurata diagnosi. Nei pazienti affetti da...
La ATCT: il trapianto di cellule T come terapia nella HLH
Prima di parlare dell'ATCT bisogna chiarire a cosa servono le cellule T e che ruolo hanno nella Linfoistiocitosi Emofagocitica. Le cellule T, anche dette CTL. Le cellule T sono i linfociti T...
Una proposta per migliorare la diagnosi e la terapia della HLH/MAS dagli Stati Uniti
Quali sono i modelli e gli approcci e come migliorare la terapia per l'HLH? Confermare una diagnosi di Linfoistiocitosi Emofagocitica (HLH) può essere difficile per diversi motivi: la rarità della...
Anakinra è efficace nel trattamento delle HLH secondarie?
Prima di Anakinra... con la ricerca sull'HLH a che punto siamo? La nostra comprensione della HLH è sicuramente progredita negli ultimi 20 anni, favorendo lo sviluppo diagnostico e terapeutico....
Caregivers: i bisogni inascoltati di coloro che assistono i malati
Chi sono i caregivers? Una recente pubblicazione scientifica riguardante i caregivers, termine inglese che indica “coloro che si prendono cura dei malati” ha catturato la mia attenzione sia perché...
Scoperto un nuovo gene coinvolto nella manifestazione clinica della HLH familiare: NBAS
Gli sforzi nell'identificare i geni associati all'HLH Nell’ultimo ventennio lo sforzo dei ricercatori nell’identificare geni associati alla sindrome dell’HLH è cresciuto esponenzialmente. Grazie a...
Terapie CAR-T e possibili complicazioni – una manifestazione clinica di HLH
Che cosa sono le terapie CAR-T? Nel 2019 l’AIFA, l’agenzia Italiana per il farmaco, ha autorizzato una nuova terapia in pazienti affetti da una particolare forma di leucemia quella linfoblastica...
Uno studio cinese delinea le cause della HLH secondaria
La Linfoistiocitosi Emofagocita secondaria (sHLH) è diagnosticataprincipalmente negli adulti in seguito a cause non del tutto identificate come tumori, infezioni o malattie autoimmuni. Sebbene...
Emofagocitosi nella HLH: un puzzle non ancora completo
L'importanza dei macrofagi e l'emofagocitosi La plasticità funzionale dei macrofagi nel rispondere agli stimoli infiammatori è centrale nella risposta immunitaria. I macrofagi rappresentano una...
Predisposizione genetica alla HLH: a che punto siamo?
La predisposizione genetica La predisposizione o suscettibilità genetica, indica una serie di caratteristiche genetiche che rendono possibile il manifestarsi di una malattia. L’analisi delle...
Gene editing: terapia promettente per l’HLH?
Che cos'è la gene editing? Può essere una possibile terapia per le malattie istiocitarie come l'HLH? Ce ne parla la Dott.ssa Fortunati in questo interessante articolo. La terapia genica nello studio...
Diagnosticare l’HLH secondaria sarà più facile grazie a un test del sangue: i risultati dei ricercatori finanziati da AILE
Nuove e fondamentali evidenze scientifiche sulla HLH Al Bambino Gesù di Roma hanno scoperto una sottopopolazione di linfociti T nel sangue la cui presenza consente di diagnosticare l'HLH secondaria...
L’HLH si manifesta sempre con un’infezione?
L’HLH è una sindrome iperinfiammatoria provocata da una incontrollata attivazione del sistema immunitario. Ma che cosa provoca la sua comparsa? È sempre un'infezione a far manifestare l'HLH?Sappiamo...
Incidenza dell’HLH: un nuovo studio epidemiologico inglese mostra un incremento
L'incidenza dell'HLH Uno dei maggiori problemi riguardanti la Linfoistiocitosi Emofagocitica è proprio quello di quantificare l’incidenza dell'HLH. Come tutti sanno l’incidenza è una relazione...
La relazione tra l’interferone alpha/beta e gamma rimane elusiva nella HLH
Il ruolo dell'interferone nella risposta immunitaria Nell’ultimo blog abbiamo parlato delle soluzioni terapeutiche emergenti per il controllo dell’iper-infiammazione nella HLH e abbiamo visto come...
L’uso di Anticorpi sintetici per il controllo dell’iperinfiammazione mediata da interferone gamma nell’HLH e nel COVID19
Le analogie dell'iperinfiammazione da HLH e COVID19 Negli ultimi due anni, molti termini medici riferiti alle malattie respiratorie quali infezioni virali, sindrome respiratoria acuta, immunità,...
Scoperto un nuovo sottotipo genetico che causa l’HLH: la proteina RhoG regola l’attivazione dei linfociti T e NK
Abbiamo descritto in più occasioni quali sono i meccanismi molecolari che conducono alla HLH familiare (fHLH). Oggi riprendiamo l’argomento perché un team internazionale di scienziati in Finlandia,...
HLH e Sepsi: un nuovo articolo mette in luce l’importanza delle cellule T (CD8+)
Malatirari L'attenzione per questa patologia In un blog dell’anno scorso ci siamo occupati della HLH e delle somiglianze e /o differenze con la Sepsi (blog febbraio 2020). Perché questa attenzione...
L’impatto psicologico e sociale della HLH primaria valutata da pazienti e dai loro familiari.
Malatirari Negli ultimi anni la ricerca medica, sta ponendo l'attenzione anche sugli aspetti sociali dei trattamenti e sull'impatto che questi hanno sulle famiglie. Questo tipo di ricerca medica è...
Informazioni utili sui vaccini per il Covid-19
FAQ VACCINI COVID-19: Risposte sul tema attraverso siti web delle organizzazioni internazionaliL’AILE tra le sue priorità ha la salute e la sicurezza dei suoi associati.Monitoriamo gli sviluppi...
I disturbi neurologici nell’HLH: una vera e propria sfida diagnostica.
Malatirari Disturbi neurologici hlh Le manifestazioni cliniche dell'HLH Le manifestazioni cliniche della HLH sono molte e a carico di diversi organi. Le sintomatologie principali sono le...
Progressi nella terapia genica dell’HLH
Malatirari La Linfoistiocitosi Emofagocitica La Linfoistiocitosi Emofagocitica (HLH) ereditaria è causata da mutazioni in geni diversi che controllano la secrezione di granuli citotossici dalle...
Emapalumab nell’HLH ricorrente e progressiva
Malatirari Emapalumab è il primo farmaco approvato negli Stati Uniti per il trattamento della Linfoistiocitosi Emofagocitica o HLH, una malattia rara, iperinfiammatoria e pericolosa per la...
HLH negli adulti: le raccomandazioni per riconoscere la Linfoistiocitosi Emofagocitica
L'importanza della tempestività La Linfoistiocitosi Emofagocitica (HLH) negli adulti può colpire tutte le fasce di età e viene ormai riconosciuta in molti casi come malattia del sistema immunitario....
Ostruzione sinusoidale: una complicanza post-trapianto ad alta letalità
Cos'è l'ostruzione sinusoidale? Come sappiamo, il trapianto di cellule staminali ematopoietiche (HSCT) rappresenta il trattamento di scelta in alcune patologie ematologiche. In questo trattamento il...
Le cellule “Natural Killer” nella HLH secondaria diventano incapaci di produrre INFγ
La storia drammatica di Manuel, una giovane promessa dell’archeologia, che si è ammalato di HLH dopo il trapianto di cellule ematopoietiche (HSCT), illustra molto bene che cos’è questa fo...
HLH negli adulti dopo il trapianto: una realtà che inganna
La storia drammatica di Manuel, una giovane promessa dell’archeologia, che si è ammalato di HLH dopo il trapianto di cellule ematopoietiche (HSCT), illustra molto bene che cos’è questa fo...
La tempesta citochinica e l’immunosoppressione in HLH e nell’infezione da COVID-19
La prestigiosa rivista medica “Lancet” ha recentemente pubblicato un articolo di Mehta et al. intitolato “COVID-19: si consideri le sindromi da tempesta citochiniche e l’immunosoppressi...
Simili ma non le stesse: diagnosi differenziale di HLH e Sepsi
HLH e Sepsi sono due patologie simili ma non identiche. Distinguerle è molto importante perché permette un intervento terapeutico precoce e mirato essenziale per la sopravvivenza dei malati. Cos’è...
La sindrome linfoproliferativa di tipo 2 associata al cromosoma X (XLP-2)
Da qualche tempo alcuni test basati sulla citometria di flusso sono all’attenzione dei ricercatori per la loro capacità di diagnosticare in maniera accurata e precocemente la HLH.
...“Via al flusso: il nuovo test per la diagnosi della HLH”
Da qualche tempo alcuni test basati sulla citometria di flusso sono all’attenzione dei ricercatori per la loro capacità di diagnosticare in maniera accurata e precocemente la HLH.
...La sorprendente variabilità geografica del gene della Perforina
In una conversazione sulla HLH, il presidente di AILE mi espresse un giorno due curiosità
...Il trapianto di cellule staminali ematopoietiche spegne il fuoco dell’HLH
In un recente articolo pubblicato nel 2018 dalla rivista Biol. Blood Marrow Transplant, sono emersi aspetti fondamentali del trapianto allogenico di cellule staminali ematopoietiche (HSCT), in pa...
Trapianto del midollo in pazienti asintomatici con HLH
Una domanda cruciale per tutti coloro che sono coinvolti nella HLH è: Cosa fare, quando in un bambino che sta bene si identificano mutazioni che causano la linfoistiocitosi emofagocitica?
...
Informazioni sul vaccino anti COVID-19
Nel file .pdf scaricabile in basso troverete le informazioni utili sui vaccini contro il Covid-19 in relazione all’HLH.


